Biofilmbildung als Antwort auf fluktuierende Umweltbedingungen in Pseudomonas aeruginosa: ein globales genetisches Konzept
Projekt abgeschlossen
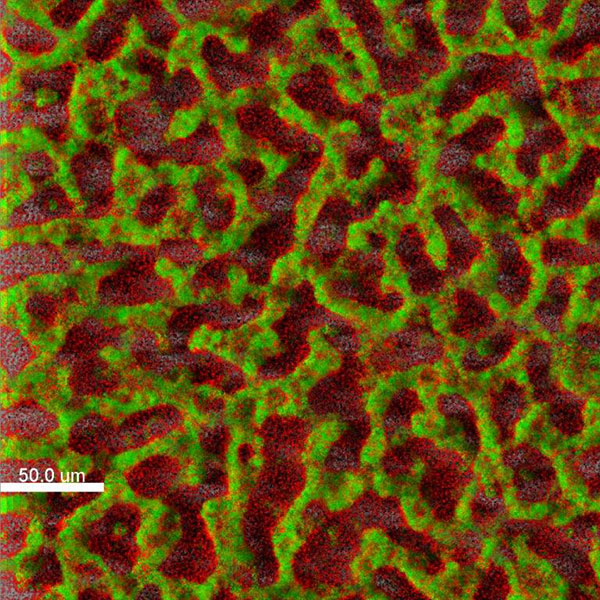
Biofilm von Pseudomonas aeruginosa
Resistenzen von Erregern gegen Antibiotika sind zu einem massiven Problem in der Medizin geworden. Immer mehr Bakterien sprechen weder auf die natürliche Immunabwehr des menschlichen Körpers an, noch auf medizinische Therapien. Das führt dazu, dass sich diese Erreger stärker ausbreiten und zu Krankheiten führen können, die kaum mehr heilbar sind. Das Bakterium Pseudomonas aeruginosa ist an vielen Infektionen beteiligt, die während eines Krankenhausaufenthaltes entstehen können („nosokomiale Infektionen“). Am Beispiel dieses Bakteriums untersucht die Forschergruppe um Susanne Häußler die Vorgänge, die zu einer dauerhaften Ansiedlung bakterieller Erreger im Menschen führen. Sie erforscht zum einen die molekularen Vorgänge im Stoffwechsel von Pseudomonas aeruginosa. Zum anderen analysiert die Arbeitsgruppe die Umweltbedingungen, unter denen dem Bakterium die dauerhafte Besiedlung des Menschen gelingt.
Bisherige Therapien stören den Stoffwechsel jedes einzelnen Bakteriums. Die Forscher hoffen, in diesem Forschungsprojekt neue Erkenntnisse über das Zusammenspiel der Bakterien als Population zu gewinnen. Eine Therapie, welche die Fähigkeit der Keime angreift, miteinander zu kommunizieren, könnte einen schnelleren Behandlungserfolg ermöglichen.
Wissenschaftliche Vorgehensweise
In diesem Projekt, das vor allem auf eigenen, bereits publizierten Ergebnissen basiert, untersuchen die Forscher den Einfluss von Umweltfaktoren auf die Expression von Proteinen, die zyklisches di-GMP (c-di-GMP) modulieren. C-di GMP ist ein weit verbreitetes, intrazelluläres Signalmolekül und eine Schlüsselkomponente in der Etablierung sessiler, bakterieller Lebensgemeinschaften ‑ sogenannter Biofilme. Bisher ist nur wenig über die Wirkungsweise von c-di-GMP bekannt. Die Untersuchungen in diesem Projekt sollen neue Erkenntnisse über die Koordinierung bakteriellen Verhaltens in der Gemeinschaft liefern.
Darüber hinaus sollen neue Zielstrukturen für alternative Anti-Infektiva identifiziert werden, welche bei chronischen Biofilm-Infektionen wirken. Im Fokus der Arbeitsgruppe stehen Strukturen, die das intrabakterielle c-di-GMP-Signalling beeinflussen. Möglicherweise kann durch die gezielte Beeinflussung der Produktion oder Degradation dieses bakterienspezifischen Signalmoleküls nicht nur in P. aeruginosa, sondern in vielen gram-negativen Pathogenen, die Regulation bakterieller Pathogenitätsmechanismen empfindlich gestört werden.
Publikationen des Forschungsprojektes A3
Kontakt

Prof. Dr. med. Susanne Häußler
TWINCORE – Zentrum für Klinische und Experimentelle Infektionsforschung
Institut für Molekulare Bakteriologie
Feodor-Lynen Str. 7
30265 Hannover
+49 511 220027-212
Susanne.Haeussler@twincore.de