Untersuchungen zur adoptiven T-Zell-Therapie mittels CMV-spezifischer γδ T-Lymphozyten nach allogener Stammzelltransplantation
Zytomegalievirus (CMV)-Infektionen bzw. Reaktivierungen sind eine häufige Ursache für Morbidität und Mortalität bei Patienten nach allogener Blutstammzelltransplantation. Ziel unseres Projekts ist es zu verstehen wie bestimmte Immunzellen, insbesondere die bisher wenig erforschten γδ T-Zellen, gegen CMV reagieren. Langfristig wollen wir herausfinden, ob und wie sich γδ T-Zellen als Zelltherapie zur Kontrolle von CMV-Infektionen einsetzen lassen. Dazu verfolgen wir in einer prospektiven klinischen Studie die Kinetik der Regeneration solcher γδ T-Zellen nach der Transplantation. Zur Bestimmung des CMV-spezifischen γδ T-Zell-Rezeptor-Repertoires in den von unseren Patienten bereitgestellten Blutproben haben wir eine moderne Hochdurchsatz-Sequenzierungs-Methode etabliert. Nach Identifizierung spezifischer γδ T-Zellen anhand des T-Zell-Rezeptor-Repertoires, wollen wir in einem weiteren Schritt die Funktionalität dieser vermutlich anti-viralen γδ T-Zellen Untersuchen. Abschließend wollen wir herausfinden, welche Virusmoleküle (Antigene) diese CMV-reaktive γδ T-Zellen mittels ihres T Zell Rezeptors erkennen.
Wissenschaftliche Vorgehensweise
γδ T-Zellen sind unkonventionelle T-Lymphozyten, die sowohl der angeboren als auch der erworbenen Immunantwort zugeordnet werden können. Da γδ T Zellen Antigene MHC-unabhängig erkennen, verursachen sie keine Graft-versus-Host-Erkrankung und haben ein hohes Potential als Immunzelltherapeutikum eingesetzt zu werden. In diesem Projekt erforschen wir das höchst diverse Repertoire ihrer klonalen rearrangierten T-Zellrezeptoren (TCR). Dazu haben wir eine RNA/cDNA-basierte Hochdurchsatz-TCR-Sequenzierungs-Methode etabliert. Zur Amplicon Generation werden γδ T-Zellen mit dem Durchflusszytometer sortiert und anschließend alle variablen (V) und konstanten (C) Regionen der humanen TRG und TRD Gene über spezifische multiplex Primer isoliert, um die CDR3 Regionen der rearrangierten TRG und TRD Ketten per PCR zu amplifizieren. Die generierten CDR3 Amplicons werden im Hochdurchsatzverfahren sequenziert und bioinformatisch analysiert.
Diese Technologie ermöglicht es uns, die Kinetik individueller γδ TCR Repertoires von Leukämiepatienten vor und nach allogener Stammzelltransplantation zu untersuchen. Unsere aktuellen Ergebnisse zeigen, dass erneuerte γδ TCR Repertoires schnell eine hohe Komplexität erlangen, obwohl sie nach Stammzelltransplantation komplett verändert sind. Wir gehen davon aus, dass diese Studienergebnisse wichtig sind um die Rolle von unkonventionellen T Zellen in der Infektabwehr nach einer Stammzelltransplantationen zu verstehen. Zudem sollen virusspezifische γδ T Zellrezeptoren von Zellen, welche nach CMV Reaktivierung expandieren, identifiziert und ihre Funktionalität charakterisiert werden. Im Weiteren können unsere Erkenntnisse zur Entwicklung einer erfolgreichen γδ T Zell-basierten Zelltherapie in Patienten nach Stammzelltransplantation mit erhöhtem CMV Reaktivierungsrisiko beitragen.

TCR repertoire visualization
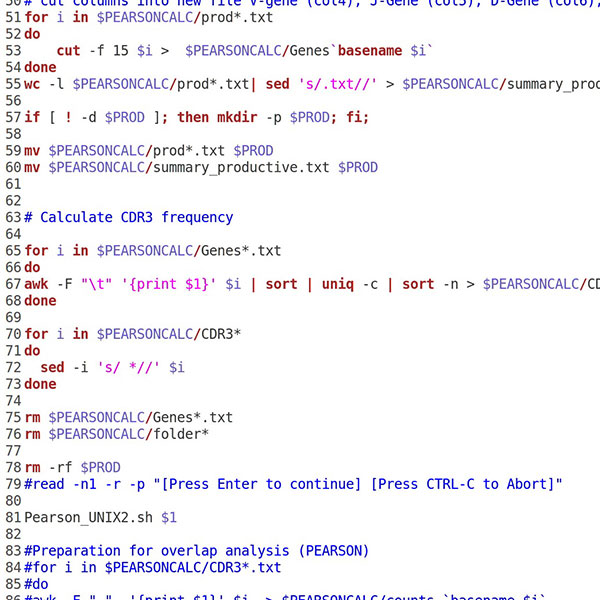
TCR repertoire analysis

Lysing T cells to extract their TCR genes
Immo Prinz und Christian Könecke erzählen über ihre Forschung im SFB 900
Immo Prinz und Christian Könecke sind dem SFB in der 2. Förderperiode im Jahr 2014 beigetreten. In ihrem Projekt B8 geht es um die Interaktion von bestimmten T-Zelltypen und dem Zytomegalievirus bei Patienten nach einer Stammzelltransplantation.
Publikationen des Forschungsprojektes B8
Kontakt

Prof. Dr. rer. nat. Immo Prinz
Institut für Immunologie
Medizinische Hochschule Hannover
Carl-Neuberg-Str. 1
30625 Hannover
+49 511 532-9739
Prinz.Immo@mh-hannover.de

Prof. Dr. med. Christian Könecke
Institut für Immunologie
Klinik für Hämatologie, Hämostasiologie, Onkologie und Stammzelltransplantation
Medizinische Hochschule Hannover
Carl-Neuberg-Str. 1
30625 Hannover
+49 511 532-3696
Koenecke.Christian@mh-hannover.de
